肺部疾病已成为全球主要的健康威胁之一。据世界卫生组织(WHO)及国际癌症研究机构(IARC)统计数据显示,每年全球约480万人因肺病死亡。由于传统治疗手段对部分难治性肺部疾病存在疗效瓶颈,开发创新型治疗技术迫在眉睫。近年来,作为细胞间通讯的重要媒介,外泌体在肺部疾病治疗领域展现出独特优势,已成为当前生物医学研究的热点方向。
一,外泌体(Exosome)
外泌体(Exosome)是细胞分泌的一种纳米级膜泡结构,直径通常在30-150nm之间。蕴含着丰富的生物活性物质,如蛋白质、核酸(mRNA、miRNA 等)、脂质等,堪称细胞间的“分子快递”。这些生物活性物质使得外泌体能够在细胞间传递信息,调节受体细胞的功能和行为。
外泌体几乎由所有细胞分泌,且广泛存在于各种体液中,如血液、尿液、唾液、乳汁等,这为其在疾病诊断和治疗中的应用提供了便利。
从结构上看,外泌体拥有完整的脂质双分子层膜结构,这层膜不仅能保护内部生物活性物质免受外界环境的破坏,还像一把 “钥匙”,上面携带的特异性蛋白可以精准识别并结合靶细胞表面的受体,确保分子能够准确送达。
这种天然的靶向性是许多人工合成药物载体难以比拟的优势,尤其对于肺部这种结构复杂、血管丰富的器官,外泌体能够避开多重生理屏障,直达病变组织,这也让外泌体成为肺部疾病治疗研究的重点方向。
而雾化方式更是让外泌体的靶向优势得到充分发挥。外泌体雾化是将外泌体制成雾化剂,通过呼吸使外泌体直接到达肺部病变部位,提高局部药物浓度,增强治疗效果。
二,外泌体对肺部疾病的作用机制
No.1抗炎与免疫调节
肺部疾病往往伴随着炎症反应,过度的炎症会导致肺组织损伤。外泌体可以通过多种途径发挥抗炎和免疫调节作用。
一方面,它能影响免疫细胞的活性,例如在急性肺损伤模型中,间充质干细胞来源的外泌体(MSC-Exos)可促使巨噬细胞从促炎的M1型向抗炎的M2型极化,从而减少炎症因子(如肿瘤坏死因子-α、白细胞介素-6等)的释放,减轻肺部炎症。
另一方面,外泌体可以直接与肺细胞表面的受体(如Toll样受体,TLR)相互作用,抑制促炎信号通路的激活,进而抑制炎症反应。对于一些自身免疫性肺部疾病,如系统性硬化症相关间质性肺病,外泌体的免疫调节功能有助于平衡失调的免疫系统,缓解疾病进展。
No.2促进组织修复与再生
外泌体携带的各种生物活性物质,如生长因子(如血管内皮生长因子、表皮生长因子等)、细胞因子等,能够刺激细胞增殖和分化。在肺部损伤后,外泌体可以促进肺泡上皮细胞、内皮细胞等的增殖和修复,加速受损肺组织的再生。
同时,外泌体还可能影响血管生成和组织重塑,为肺组织的修复提供良好的微环境。例如在肺纤维化模型中,外泌体能够通过激活相关信号通路,促进肺泡上皮细胞的再生,减少纤维化组织的形成,改善肺功能。
No.3抗纤维化作用
肺纤维化是一种严重的肺部疾病,其特征是肺组织进行性瘢痕化,导致肺功能逐渐丧失。外泌体在抗纤维化方面表现出显著的潜力。
研究发现,外泌体中的一些miRNA能够有效抑制转化生长因子-β(TGF-β)和Wnt/β-连环蛋白等纤维化相关信号通路,阻断成纤维细胞的活化和胶原蛋白的过度沉积,从而延缓肺纤维化的进程。
此外,外泌体还可以通过调节细胞外基质的代谢,促进纤维化组织的降解和重塑,对已经形成的纤维化病灶也有一定的改善作用。
No.4作为药物载体的精准治疗
外泌体具有低免疫原性和良好的生物相容性,这使其成为一种理想的药物载体。将治疗药物(如小分子药物、蛋白质药物、核酸药物等)装载到外泌体中,可以实现药物的精准递送。
通过对肺部疾病相关细胞表面标志物的研究,设计能够靶向这些标志物的外泌体,使其能够特异性地将药物输送到肺部病变部位,提高药物的疗效,同时减少药物对其他组织和器官的副作用。
三,外泌体在肺部治疗中的临床研究

治疗肺纤维化的突破
近年来,多项关于外泌体治疗肺纤维化的研究取得了突破性进展。
2025年6月,清华大学精准医学研究院联合解放军总医院等机构团队,在国际医学权威期刊《Signal Transduction and Targeted Therapy》公布了人体临床试验结果,证实干细胞外泌体雾化治疗可安全逆转肺纤维化进程。
该研究纳入了24名患者,随机接受7天的人脐带间充质干细胞衍生的细胞外囊泡(hUCMSC-EVs)雾化治疗或安慰剂对照。
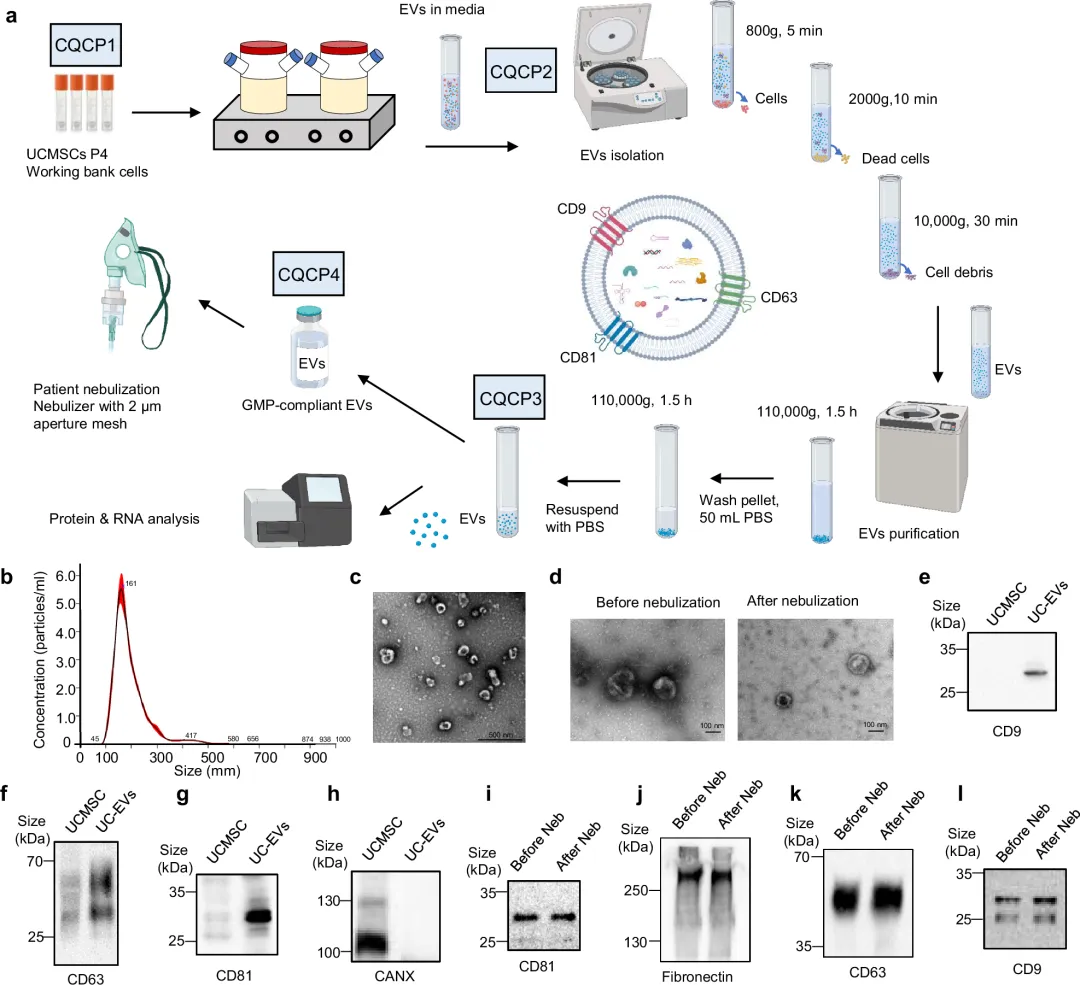
结果显示,所有患者耐受良好,未出现严重不良事件。接受hUCMSC-EVs治疗的患者肺功能显著改善,用力肺活量(FVC)和最大自主通气量(MVV)显著提升。圣乔治呼吸问卷(SGRQ)评分明显降低,表明患者生活质量提升。特别值得注意的是,两名患者的薄层CT显示纤维化病灶大幅度消退,这为肺纤维化患者带来了新的希望。
改善其他肺部疾病的研究进展
以下为外泌体雾化治疗不同肺部疾病的研究进展:
系统性硬化病(SSc)相关间质性肺病
此类疾病会导致肺部组织逐渐纤维化,影响呼吸功能。
有研究团队尝试采用外泌体雾化方式对相关患者进行治疗,通过间充质干细胞来源的细胞外泌体(MSC-EVs)雾化给药。
治疗后,患者的临床症状明显改善,呼吸困难和干咳减少,不再需要吸氧,复查胸部CT结果显示毛玻璃样实变和纤维化改变明显减少。
哮喘
哮喘是一种以气道慢性炎症、气道高反应性和气道重塑为特征的异质性疾患,其病理生理核心在于免疫失衡与结构重塑的恶性循环。
在哮喘动物模型中,外泌体已被证实可通过多维度机制发挥治疗作用。例如间充质干细胞来源的外泌体(MSC-EVs)能显著降低支气管肺泡灌洗液(BALF)中总细胞数及嗜酸性粒细胞比例,减少Th2型细胞因子分泌。
国内一项针对重度哮喘的临床研究显示,一名23岁男性患者(每日需依赖支气管扩张剂)接受间充质干细胞外泌体(MSC-EVs)雾化治疗(剂量:2×10^9个外泌体/次,每日1次,连续5天)后,气道高反应性降低60%,过敏原诱发的气道炎症指数下降54%。随访1年期间,患者未出现急性发作,常规药物剂量减半,生活质量评分(AQLQ)提高3.2倍。
慢性阻塞性肺疾病(COPD)
COPD以持续气流受限和呼吸道症状为特征,常伴有气道和肺组织的慢性炎症。
中国科学家团队在《Cellular Immunology》期刊发表的研究显示,间充质干细胞外泌体(MSC-EVs)通过雾化吸入可精准修复COPD大鼠模型的受损肺组织。
在香烟烟雾与脂多糖诱导的COPD模型中,低剂量外泌体雾化组(0.5×10⁸ particles/kg)的肺功能指标FEV0.2/FVC恢复至接近正常水平,促炎因子TNF-α、IL-6降幅超50%,抗炎因子IL-10水平显著提升。雾化给药使病灶局部药物浓度提升3-5倍,生物利用度高达78%,优于静脉注射。
急性肺损伤(ALI)/ 急性呼吸窘迫综合征(ARDS)
ALI和ARDS是严重的肺部急症,大量基础研究表明间充质干细胞来源的外泌体治疗,能促使巨噬细胞极化改变,减少炎症因子释放,促进相关细胞修复再生等。
全球首项针对重症COVID-19相关ARDS的雾化外泌体治疗研究显示,7例重症患者(4男3女,中位年龄57岁)接受连续5天雾化吸入人异体间充质干细胞外泌体(haMSCs-Exos,剂量2.0×10⁹纳米囊泡/日)后,肺部病变显著消退,其中4例改善明显。
患者淋巴细胞计数增加(中位数1.61×10⁹/L vs. 1.78×10⁹/L),炎症指标如C反应蛋白(CRP)、白细胞介素6(IL-6)、乳酸脱氢酶(LDH)均呈下降趋势,且无严重不良事件发生。所有患者均在治疗后20天内出院。
肺动脉高压(PH)
PH是一种以肺动脉压力升高为特征的疾病,科研层面已发现外泌体可调节肺动脉平滑肌细胞增殖和凋亡、抑制血管重构等。
国内首例PH患者(女性,58岁,肺动脉平均压55mmHg),在接受MSC-EVs雾化治疗(每周2次,连续4周)后,6分钟步行距离从180米提升至320米,NT-proBNP水平下降80%,肺动脉造影显示血管重构明显逆转。
国际期刊《Stem Cells Translational Medicine》报道的3例PH患者,经外泌体雾化治疗后,运动耐量(通过心肺运动试验评估)提升40%,肺动脉楔压(PAWP)降低35%。
综上所述,外泌体作为天然的细胞间通讯载体,凭借其独特的靶向性、低免疫原性及多功能活性物质负载能力,在肺部疾病治疗领域展现出革命性潜力。未来,外泌体医学的深入发展或将重塑呼吸系统疾病的治疗格局,开启细胞外囊泡治疗的新纪元。
免责声明:凡本平台转载的文章、图片、音频、视频等资料的版权均归版权所有人所有,如有侵权,请联系我们删除,带来不便,敬请谅解!我们旨在科普相关知识,传递行业前沿进展,本文观点不作为医疗指导建议,无推荐公司和医院之意,如需就医请咨询正规医院医生。
